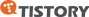리소좀(Lysosome)은 단백질 분해 효소가 들어있는 세포 내의 작은 주머니이다.
일반적으로 오래되어서 못 쓰게 된 세포소기관을 파괴하거나 외부에서 탐식작용을 통해 먹어 치운 바이러스나 박테리아 같은 외부 물질들을 파괴하는 데에 사용된다.
일반적으로 리소좀 내부는 상당히 낮은 pH 조건을 유지하고 있다.
1955년 드 뒤브 등은 쥐의 간세포 마쇄액(磨碎液)을 원심 분리하자 미토콘드리아보다 약간 가볍고, 마이크로좀보다 약간 무거운 미소 과립을 얻을 수 있다는 것을 발견했다.
그들은 이 과립을 리소좀이라고 불렀다.
리소좀에는 여러 종류의 산성 가수분해 효소(산성 포스파타아제·산성 리보뉴클레아제 따위)가 들어 있다.
리소좀은 전자 현미경으로 보면 한 겹의 막으로 싸인, 지름 0.5μm 정도의 공모양이다.
리소좀은 0.1~1.2μm까지 다양한 크기를 가지고 있다.
리소좀과 유사한 구조를 가진 것으로 마이크로바디라는 과립이 있다.
이 소체는 과밀화 효소를 함유하고 있기 때문에 파오키시좀이라고도 한다.
따라서 리소좀을 전자 현미경적으로 고정하려면 산성 포스파타아제의 활성이 있고, 더욱이 한 겹의 외막을 가진 것을 확인하면 된다.
왜냐하면 리소좀을 함유하는 모든 효소를 세포 화학적으로 검출하기는 매우 어렵기 때문이다.
리소좀은 동물의 여러 가지 세포에 널리 분포하지만 식물 세포에서는 아직 확실하지 않다.
리소좀은 식세포나 백혈구 등 식작용이 활발한 세포에 많이 있다.
리소좀의 기능은 산성하에서 소화에 관계한다고 볼 수 있다.
리소좀 축적질환이란 유전적 원인에 의해 이러한 효소들 중 일부가 정상적으로 기능을 하지 못하게 되면서 분해되지 못한 물질이 리소좀 내에 축적되고, 그 결과 신체 조직과 장기에 이러한 물질을 다량으로 포함한 비정상적 세포가 늘어나면서 다양한 이상증상이 발생하는 질환이다.
'질병정보' 카테고리의 다른 글
| 쇼그렌 증후군 (0) | 2019.03.11 |
|---|---|
| 봄의 불청객, ‘알레르기성 결막염’ (0) | 2019.03.11 |
| 소음성 난청 (0) | 2019.03.05 |
| 봄에는 'A형간염' 조심 (0) | 2019.03.04 |
| 골육종 (0) | 2019.02.26 |